لقد صادفنا جميعًا كلمة "نشاط إشعاعي" في مكان ما أو آخر. هل تعرف أن النظير هو أساس النشاط الإشعاعي؟ في كثير من الأحيان ظهرت مصطلحات مثل الطاقة النووية والمفاعلات النووية والأسلحة النووية في الأخبار والكتب المدرسية. لكن ما هو النشاط الإشعاعي وكيف يرتبط بالنظائر؟
النشاط الإشعاعي هو أحد خصائص الذرات. سيكون لكل ذرة مشعة نواة غير مستقرة. وبالتالي فإنه يميل إلى إطلاق جزيئات دون ذرية للحصول على الاستقرار وبالتالي إطلاق الإشعاع أو الطاقة في العملية. العناصر أو الذرات موجودة في كل من الأنواع المشعة وغير المشعة.
سيكون عدد النيوترونات في كلا الصنفين مختلفًا. هذه الأنواع المختلفة من نفس العنصر تسمى النظير. اقرأ هذه المقالة لمعرفة المزيد عن النظائر.
تعريف النظائر
تُعرف العناصر التي لها نفس العدد الذري ولكن تختلف في العدد الكتلي وتسمى بأنها "نظائر". يُطلق على عدد البروتونات والنيوترونات مجتمعة معًا الكتلة الذرية (العدد الكتلي) أو عدد كتلة العنصر ، بينما يطلق على العدد الإجمالي للبروتونات بالعدد الذري للعنصر.
لكي لا تختلط عليك الأمور عليك أن تعرف أن نظائر العنصر لها:
- نفس العدد الذري
- تختلف في العدد الكتلي
في عنصر معين ، سيبقى عدد البروتونات ثابتًا دائمًا. ومع ذلك ، يمكن أن يتغير عدد النيوترونات. يختلف عدد النيوترونات ولكن عدد البروتونات يظل ثابتًا في نظير عنصر واحد. وبالتالي ، فإن تعريف "العناصر التي لها نفس العدد الذري ولكن عدد كتلة مختلف تسمى النظائر". فمثلا
1. نظائر الهيدروجين H
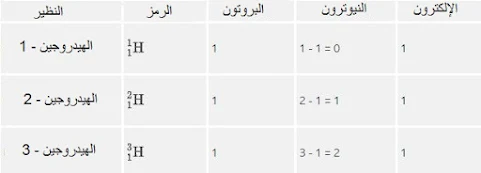
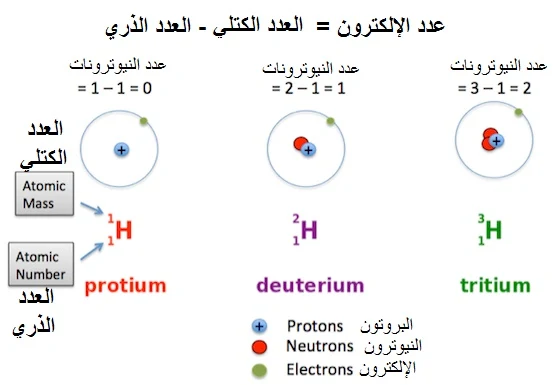
يحتوي الهيدروجين hا على ثلاثة أشكال نظيرية أكثر استقرارًا - البروتيوم والديوتيريوم والتريتيوم. تحتوي جميع الأشكال النظيرية الثلاثة للهيدروجين على نفس عدد البروتونات ولكنها تختلف في عدد النيوترونات. عدد النيوترونات في البروتيوم هو صفر ، وعدد النيوترونات في الديوتيريوم واحد ، وعدد النيوترونات في التريتيوم هو اثنان. يمكنك ملاحظة ذلك في الجدول.
يمكنك ملاحظة ذلك في الرسم أدناه
2. نظائر الكربون C
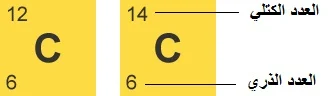
يحتوي الكربون على ثلاثة أشكال نظيرية - الكربون 12 ، والكربون 13 ، وكذلك الكربون 14. تمثل الأرقام 12 و 13 و 14 الكتل الذرية (أي العدد الكتلي) لأشكال نظيرية مختلفة من الكربون. كما تمت مناقشته ، الرقم الذري هو الخاصية الفريدة التي يمكننا من خلالها تحديد العنصر. لذلك ، فإن العدد الذري 6 للكربون في جميع الأشكال ثابت. الكربون 12 هو النظير المستقر لعنصر الكربون بينما الكربون 14 هو النظير المشع.
يتم إعطاء الكتل الذرية النسبية في الجدول الدوري. لديهم الرمز Ar.
احرص على عدم الخلط بين الأعداد الكتلية والكتلة الذرية النسبية:
الأعداد الكتلية هي دائمًا أعداد صحيحة (لا يمكن أن يكون لديك جزء من بروتون أو نيوترون)
غالبًا ما يتم تقريب الكتل الذرية النسبية إلى أقرب عدد صحيح ، ولكنها في الواقع ليست أعدادًا صحيحة
على سبيل المثال ، الكتلة الذرية النسبية للكلور هي 35.5 وليس عددًا صحيحًا. وذلك لأن الكلور يحتوي على نظيرين مختلفين ، الكلور 35 والكلور 37.
تصفح المزيد من المواضيع عن التركيب الذري والجزيئي:
أمثلة على النظائر
- أشكال نظائر الأكسجين - أكسجين - 16 ، أكسجين - 17 ، أكسجين - 18
- الأشكال النظيرية لليورانيوم: U-235 ، U-238
- الكلور - 35 ، الكلور - 37 هي الأشكال النظيرية للكلور
- الأشكال النظيرية للفلور: الفلور 17 ، الفلور 18 ، الفلور 19
- الهيدروجين - 1 ، الهيدروجين - 2 ، الهيدروجين - 3 هي الأشكال النظيرية للهيدروجين
- الأشكال النظيرية للكربون : الكربون- 12 ، الكربون - 13 ، الكربون - 14
يوجد ما يقرب من 275 نظيرًا مختلفًا لـ 81 عنصرًا مستقرًا. يوجد أكثر من 800 نظير مشع طبيعي وصناعي. يمكن أن يحتوي عنصر واحد موجود في الجدول الدوري على عدة أشكال نظيرية.
1. الخواص الكيميائية للنظائر
بشكل عام ، تكون الخصائص الكيميائية لنظائر أي عنصر متطابقة تقريبًا. الاستثناء في هذه الحالة هو نظائر الهيدروجين لأن عدد النيوترونات لها تأثير كبير على حجم نواة ذرة الهيدروجين.
2. الخصائص الفيزيائية للنظائر
تختلف الخصائص الفيزيائية للنظائر في عنصر معين عن بعضها البعض. وذلك لأن الخصائص الفيزيائية لأي نظير تعتمد على الكتلة. تختلف كتلة كل نظير لعنصر واحد عن بعضها البعض. تُستخدم عمليات مثل التقطير التجزيئي والانتشار لفصل النظائر عن بعضها البعض. نحن نستفيد من حقيقة أن النظائر لها خصائص فيزيائية مختلفة.
استخدامات النظائر
- يستخدم التأريخ الكربوني الكربون 14 ، وهو أحد نظائر الكربون. يوجد هذا النظير للكربون في الغلاف الجوي ككربون مشع. تساعد كمية الكربون 14 التي تم الحصول عليها في الحفريات علماء الحفريات على حساب عمر الحفريات.
- تشتهر نظائر اليورانيوم باستخدامها في المفاعلات النووية. يستخدم اليورانيوم 235 كوقود في المفاعلات النووية.
- تستخدم النظائر المشعة للأغراض الطبية. وهي تستخدم للكشف عن الأورام والجلطات الدموية وما إلى ذلك. الزرنيخ 74 ، وهو أحد نظائر الزرنيخ ، ويستخدم لتحديد وجود الورم. وبالمثل ، يستخدم الصوديوم 24 للكشف عن جلطات الدم.
- يستخدم نظير الكوبالت (الكوبالت -60) للكربون في علاج السرطان.
- يساعد نظير اليود (اليود 131) للكربون في علاج تضخم الغدة الدرقية.
تحديد نظائر العنصر
يمكن تعريف نظير عنصر ما على أنه أحد المتغيرات المتعددة للعنصر الكيميائي المحدد الذي يحمل نفس عدد البروتونات والإلكترونات مثل العدد الذري للعنصر ولكنه يحتوي على عدد مختلف من النيوترونات عند مقارنته بالمتغيرات الأخرى (النظائر) للعنصر. بالتناوب ، يمكن تعريف النظائر على أنها متغيرات من العناصر التي تختلف في أعداد النيوكليون الخاصة بها بسبب اختلاف في العدد الإجمالي للنيوترونات في نواتها.
سؤال محلول لك
سؤال: تختلف نظائر عنصر واحد في عدد
1. نيوترونات
2. البروتونات
3. الإلكترونات
4. كل ما ورداعلاه
الجواب: رقم 1 (نيوترونات). سيكون عدد البروتونات ثابتًا دائمًا في عنصر واحد. ومع ذلك ، يمكن أن يتغير عدد النيوترونات. يختلف عدد النيوترونات في نظائر العنصر ، لكن عدد البروتونات يظل ثابتًا دائمًا.
أهم المصادر: